上海研匠生物科技有限公司
4 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
上海研匠生物科技有限公司
入驻年限:4 年
- 联系人:
陈经理
- 所在地区:
上海 闵行区
- 业务范围:
试剂、抗体、ELISA 试剂盒、技术服务、论文服务、细胞库 / 细胞培养
- 经营模式:
经销商 代理商 生产厂商 科研机构
技术资料/正文
STTT|哈尔滨医科大学杜伟杰 / 杨宝峰团队揭示心肌梗死来源外泌体抑制肿瘤铁死亡促进肿瘤进展新机制
103 人阅读发布时间:2026-03-11 11:19
心力衰竭(HF)与癌症作为全球两大致命疾病,存在密切的病理关联,心肌梗死(MI)诱发的心力衰竭被证实可显著增加肿瘤发生风险并加速肿瘤进展,但二者之间的远程调控机制尚未明确。铁死亡作为一种铁依赖的非凋亡性细胞死亡方式,已成为癌症治疗的潜在靶点,而肿瘤对铁死亡的抵抗是临床治疗面临的重要挑战。外泌体作为细胞间通讯的关键媒介,可携带 miRNA 等生物活性分子介导远程器官调控,但其在心肌梗死与肿瘤铁死亡敏感性调控中的作用及分子机制仍有待阐明。(外泌体提取妍泌生物可提供外泌体试剂盒)
哈尔滨医科大学杜伟杰教授、杨宝峰教授团队在《Signal Transduction and Targeted Therapy》(IF:38.1)发表题为 “Exosomes secreted from cardiomyocytes suppress the sensitivity of tumor ferroptosis in ischemic heart failure” 的研究论文。该研究首次发现心肌梗死诱发心力衰竭后,心肌细胞分泌的外泌体可通过递送 miR-22-3p 靶向抑制肿瘤细胞中促铁死亡基因 ACSL4 的表达,降低肿瘤细胞对铁死亡诱导剂的敏感性,最终促进肿瘤生长。该研究揭示了 “心脏 - 肿瘤” 跨器官病理通讯的全新机制,为心肌梗死合并肿瘤患者的精准治疗提供了新的分子靶点与治疗策略。

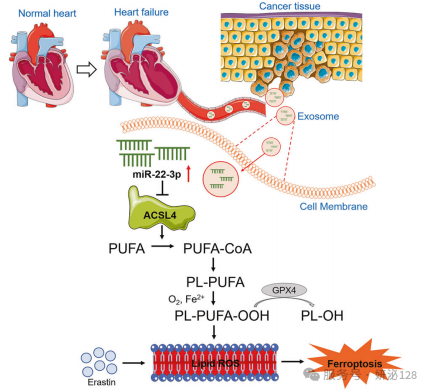
为探究心肌梗死后心力衰竭(post-MI HF)对肿瘤细胞铁死亡敏感性的影响,研究构建假手术 / 心梗联合肿瘤异种移植小鼠模型,采用铁死亡激活剂 erastin和IKE 干预,通过心脏超声检测心功能、检测心衰标志物表达,同时检测肿瘤体积 / 重量,并结合免疫组化、分子检测分析肿瘤组织铁死亡相关指标;结果发现心梗小鼠心功能显著受损、心衰标志物上调,erastin/IKE 未加重心脏损伤,且心梗会加速肿瘤生长,erastin/IKE 可显著抑制假手术组小鼠肿瘤生长,但该抑制作用在心梗小鼠中被大幅削弱,同时心梗显著降低了 erastin/IKE 诱导的肿瘤组织铁死亡相关标志物表达,证实心梗诱导的心力衰竭在体内会抑制肿瘤细胞对铁死亡的敏感性。
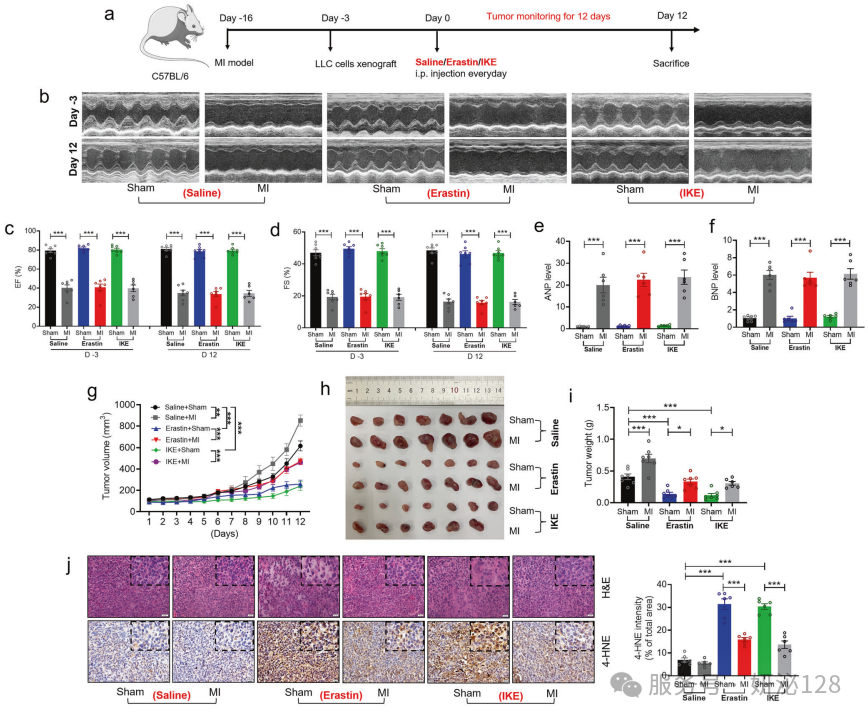
2.外泌体对erastin诱导的体内肿瘤铁死亡的影响
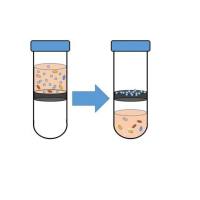
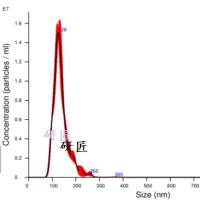
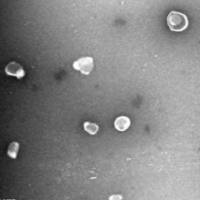
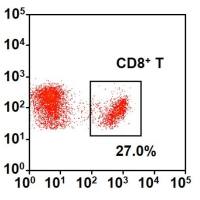
为探究心梗诱导的心力衰竭调控肿瘤铁死亡敏感性的机制,研究构建心梗致心衰小鼠模型,通过超速离心结合外泌体提取试剂盒分离假手术组和心梗组小鼠的血浆外泌体,经电镜、蛋白印迹、纳米颗粒追踪分析鉴定外泌体特征,再向荷瘤裸鼠连续输注等量假手术组 / 心梗组血浆外泌体并联合 erastin 干预,检测肿瘤生长及铁死亡、增殖相关指标,同时在 C57BL/6 小鼠中验证结果;结果发现心梗组血浆外泌体的颗粒密度更高,两组外泌体粒径均符合典型范围,erastin 可诱导肿瘤脂质过氧化并显著抑制肿瘤生长,而心梗组血浆外泌体可明显逆转该效应,假手术组外泌体则无此作用,且该结果在 C57BL/6 小鼠中得到验证,证实心梗诱导的心衰来源血浆外泌体可降低肿瘤对 erastin 诱导的铁死亡的敏感性。
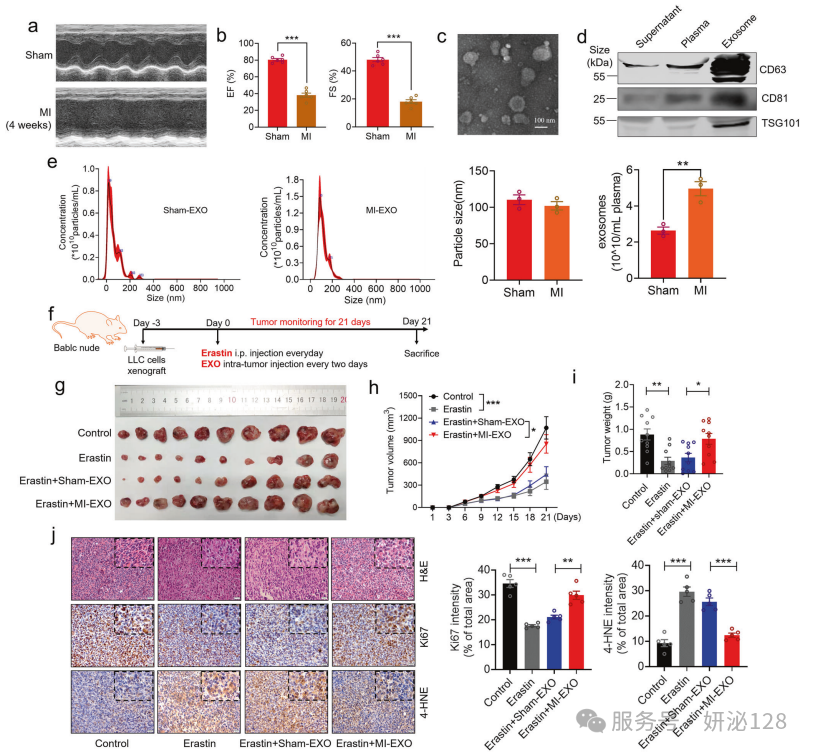
3.外泌体对erastin诱导的体外肿瘤细胞铁死亡的影响
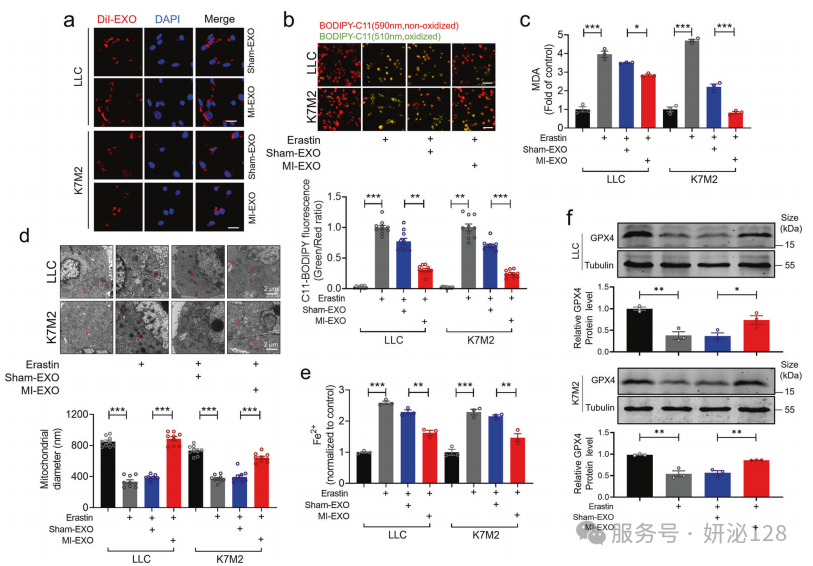
为探究心梗来源外泌体(MI-EXO)调控肿瘤细胞铁死亡的体外作用及相关机制,研究分离假手术组外泌体(Sham-EXO)与 MI-EXO,将其分别与小鼠 LLC 肺癌细胞、K7M2 骨肉瘤细胞共培养,通过荧光标记验证外泌体与肿瘤细胞的融合能力,结合脂质活性氧检测、MDA 含量测定、电镜观察、铁离子检测、蛋白印迹及集落形成、细胞增殖 / 侵袭 / 迁移实验,同时联用铁死亡抑制剂 Fer-1 开展验证实验;结果发现外泌体可高效融合肿瘤细胞,MI-EXO 能显著抑制 erastin 诱导的肿瘤细胞脂质 ROS 蓄积、铁死亡发生,逆转 erastin 导致的线粒体超微结构异常,降低细胞内 Fe²+ 水平、恢复 GPX4 蛋白表达,还能恢复肿瘤细胞集落形成能力,缓解 erastin 对肿瘤细胞增殖、侵袭和迁移的抑制作用,且 Fer-1 联合 MI-EXO 可进一步削弱 erastin 对肿瘤细胞侵袭迁移的抑制,证实 MI-EXO 可在体外直接抑制肿瘤细胞的铁死亡进程。
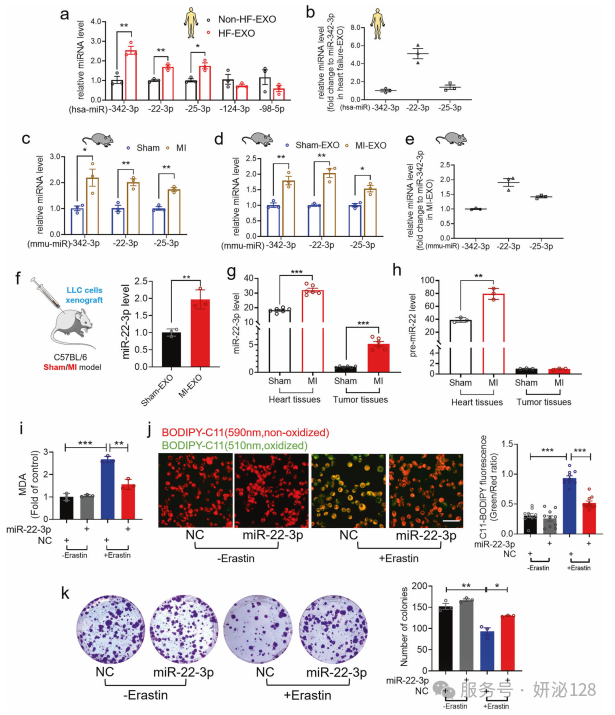
4.HF衍生外泌体miR-22-3p抑制肿瘤铁死亡
为探究心梗致心衰来源外泌体调控肿瘤铁死亡敏感性的核心分子机制,研究通过miRNA芯片分析获得数据心衰外泌体中高丰度的 5 种 miRNA,通过 qRT-PCR 验证其在人心衰患者及小鼠心梗模型的心肌组织、血浆外泌体中的表达,结合数据库分析明确核心候选 miRNA,再检测心梗荷瘤小鼠的外泌体及心、肿瘤组织中该 miRNA 的表达水平,最后通过体外过表达等实验,检测肿瘤细胞铁死亡相关指标及集落形成能力;结果发现 miR-22-3p 是人心衰患者和小鼠心梗模型外泌体中丰度最高的差异 miRNA,其在心梗小鼠心肌组织、血浆外泌体及荷瘤小鼠肿瘤组织中均显著上调,证实该 miRNA 由心梗心肌通过外泌体分泌至肿瘤组织,体外实验显示过表达 miR-22-3p 可显著抑制 erastin 诱导的肿瘤细胞铁死亡,抑制该 miRNA 则作用相反,证实心梗致心衰来源外泌体中的 miR-22-3p 是介导肿瘤细胞铁死亡敏感性降低的关键分子。
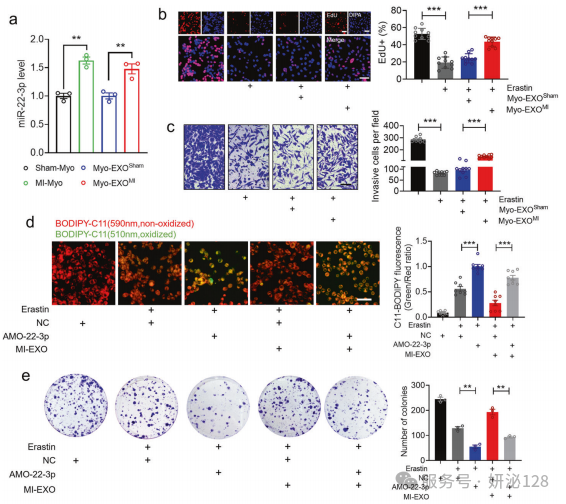
5.心肌细胞来源的外泌体miR-22-3p抑制肿瘤细胞铁死亡
为验证心梗后心衰血浆外泌体调控肿瘤铁死亡的效应源于受损心肌细胞且由 miR-22-3p 介导,研究分离假手术 / 心梗小鼠心肌细胞及心肌来源外泌体,结合细胞转染、构建心肌特异性 miR-22-3p 海绵体 AAV9 载体等实验,检测 miR-22-3p 表达、肿瘤细胞铁死亡相关指标及荷瘤小鼠肿瘤生长情况;结果发现心梗心肌细胞及其外泌体中 miR-22-3p 高表达,其可恢复 erastin 对肿瘤细胞的抑制作用,敲低 miR-22-3p 能增强肿瘤细胞铁死亡、部分逆转心梗外泌体的抗铁死亡效应,心肌特异性敲低 miR-22-3p 不影响心功能但可显著减小心梗荷瘤小鼠肿瘤体积,证实心梗后心衰血浆外泌体的抗铁死亡效应主要来自受损心肌细胞的外泌体,miR-22-3p 是介导该效应的核心分子,靶向敲低心肌来源的 miR-22-3p 可恢复肿瘤铁死亡敏感性并发挥抗肿瘤作用。
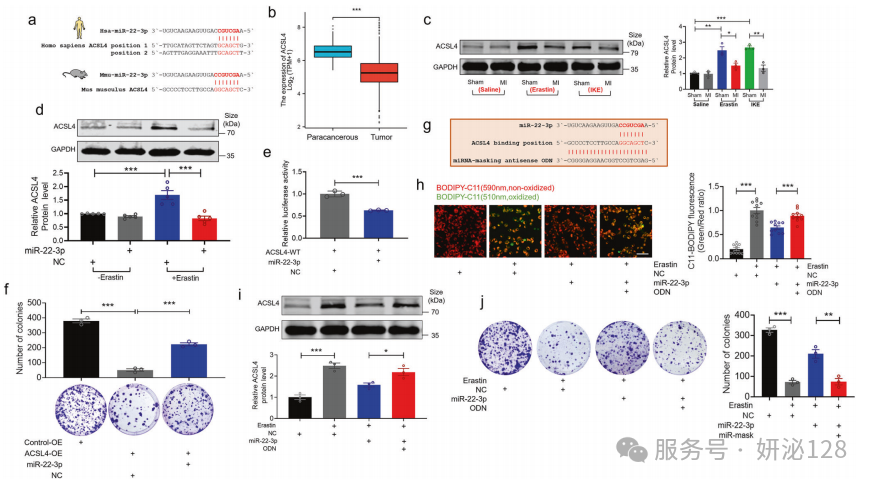
6.miR-22-3p与铁死亡相关基因ACSL4的直接相互作用
为探究 miR-22-3p 调控肿瘤细胞铁死亡的下游靶基因及作用机制,研究通过 Starbase 结合 Ago CLIP-seq 数据预测其潜在靶基因,结合数据库分析、蛋白印迹、荧光素酶报告基因、质粒过表达、miR-Mask 等实验验证靶基因及调控关系;结果发现 ACSL4 是 miR-22-3p 的候选靶基因,心梗会抑制 erastin/IKE 诱导的肿瘤组织 ACSL4 表达,miR-22-3p 可直接结合 ACSL4 并抑制其表达,过表达 ACSL4 可逆转 miR-22-3p 对肿瘤细胞集落形成的促进作用,阻断 miR-22-3p 与 ACSL4 的结合可恢复 erastin 诱导的铁死亡相关表型,证实 miR-22-3p 通过靶向抑制 ACSL4 表达,进而抑制 erastin 诱导的肿瘤细胞铁死亡。
本研究完整揭示了 “心肌梗死→心肌细胞分泌外泌体增多→外泌体携带 miR-22-3p 靶向肿瘤细胞→抑制 ACSL4 表达→阻断脂质过氧化→降低肿瘤铁死亡敏感性→促进肿瘤进展” 的全新致病机制,首次阐明了心肌梗死诱发心力衰竭促进肿瘤进展的远程调控通路。该研究不仅深化了对 “心脏 - 肿瘤” 跨器官病理通讯的理解,还为心肌梗死合并肿瘤患者的治疗提供了新的干预靶点,提示靶向抑制外泌体 miR-22-3p 或激活 ACSL4 可增强肿瘤对铁死亡治疗的敏感性,为临床优化肿瘤治疗策略提供了重要的实验依据。
相关文献
Yuan, Y., Mei, Z., Qu, Z. et al. Exosomes secreted from cardiomyocytes suppress the sensitivity of tumor ferroptosis in ischemic heart failure. Sig Transduct Target Ther 8, 121 (2023).
妍泌生物是专注于外泌体技术服务的创新型生物科技企业,深耕外泌体试剂研发与技术服务领域,以探索外泌体生命奥秘为使命,持续为生命科学与生物医药创新赋能。
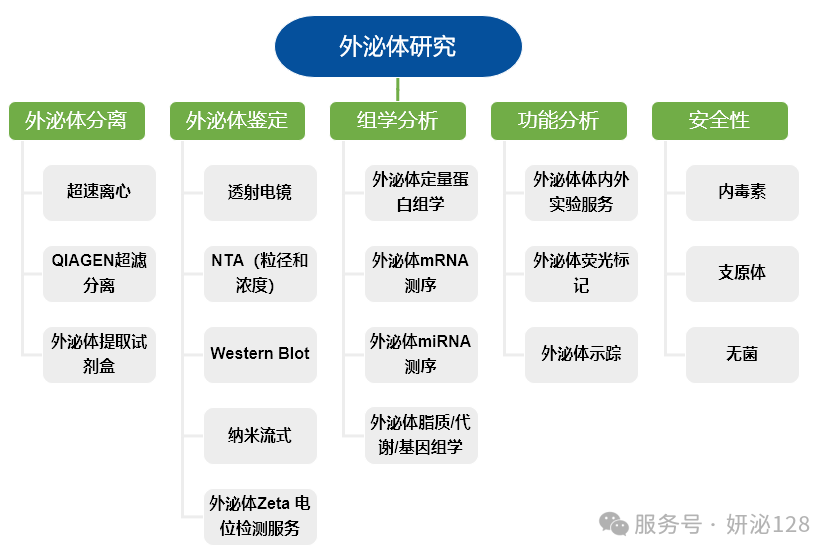
妍泌生物以技术为核心、以品质为信仰,致力于打造外泌体行业领先的试剂品牌与技术服务平台,不断优化产品体系、升级服务能力,推动外泌体技术从基础研究走向产业应用。面向高校、医疗机构及生物医药企业,公司提供全链条外泌体产品与一站式技术服务,助力科研提速、成果转化与项目落地,携手合作伙伴共拓外泌体领域新未来。
| 工作邮箱:yanjiangbio@163.com
| 官网链接:www.rcnbio.com